Что называют веществами
Из веществ, которые нас окружают, состоят все предметы в мире, например: металлический ключ, кусок сахара, воздух.
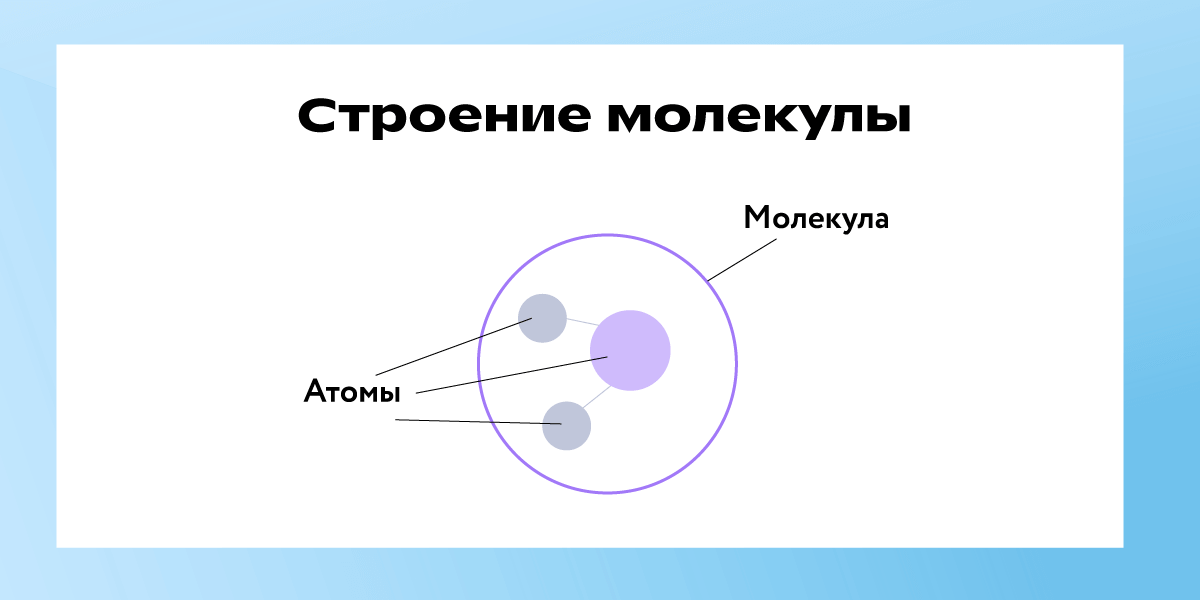
При помощи современных приборов учёные установили, что вещества состоят из атомов и молекул.
Атомы — это мельчайшие химически неделимые частицы элементов, которые соединяются в молекулы.
Атомы можно сравнить с кирпичиками, а молекулы — со стеной.
Основные классификации
Число веществ в окружающем мире поражает воображение: их больше 275 миллионов. Чтобы не запутаться в огромном разнообразии веществ в окружающем мире, учёные распределяют их по группам.
Простые и сложные вещества
Этот список веществ основан на том, из атомов скольких химических элементов состоит вещество:
- Простые вещества состоят из атомов только одного химического элемента. Например, в железном гвозде только атомы железа (Fe), в алюминиевую фольгу входят атомы алюминия (Al).
- Сложные состоят из атомов двух и более элементов в определённой пропорции. Так, кристаллы поваренной соли построены из атомов натрия (Na) и хлора (Cl) и вместе образуют хлорид натрия (NaCl). Такие вещества ещё называют химическими соединениями.
Органические и неорганические
Ещё одна важная классификация основана на происхождении и составе:
-
Органические вещества встречаются преимущественно в живой природе. В основе их структуры — цепи атомов углерода (C). Типичные представители — белки, жиры, углеводы. Другие вещества с углеродом тоже могут относиться к этой группе, например полимеры вроде пластмасс.
-
Неорганические включают практически всё остальное. Это металлы, минеральные соли, кислоты, основания, оксиды металлов и многое другое.
Твёрдые, жидкие, газообразные
Любое вещество способно находиться в трёх основных агрегатных состояниях:
-
Твёрдое тело имеет фиксированную форму и объём. Атомы и молекулы расположены близко друг к другу и связаны прочными силами взаимодействия. Так, металл, лёд и гранит не разрушатся, если на них несильно надавить.
-
Жидкость обладает постоянным объёмом, но принимает форму сосуда, в котором находится. Частицы движутся свободно, заполняя пространство. К этой категории можно отнести воду, ртуть, нефть.
-
Газ занимает весь доступный объём и обладает минимальной плотностью. Так, расстояние между частицами воздуха или гелия значительно больше, чем в твёрдых телах и жидкостях. Например, воздух и гелий свободно распространяются по помещению и могут быть значительно сжаты под давлением. Если из воздушного шарика выпустить гелий, он мгновенно рассеется в атмосфере, а объём воздуха в велосипедной камере можно уменьшить, надавив на насос.
Вещество может переходить из одного агрегатного состояния в другое в зависимости от температуры и давления.
Например, вода превращается в лёд при охлаждении и в пар при нагреве.

Ниже представлена классификация веществ в виде таблицы.
| Признак | Классификация | Пример | |
| По типу соединения друг с другом химических элементов | простые | вещества, образованные атомами только одного типа химического элемента |
водород (H2) |
| сложные | вещества, молекулы которых состоят из атомов двух или более разных химических элементов | вода (H₂O) углекислый газ (CO₂) |
|
| По происхождению и составу | органические | вещества, в состав которых входят цепи атомов углерода (C) | метан (CH4) этанол (C2H5OH) все белки, жиры и углеводы |
| неорганические | все вещества, которые не являются органическими | металлы минеральные соли кислоты основания |
|
| По агрегатному состоянию | твёрдые | имеют фиксированную форму и объём | металл лёд гранит |
| жидкие | обладают постоянным объёмом, но принимают форму сосуда | вода ртуть нефть |
|
| газообразные | занимают весь доступный объём и обладают минимальной плотностью | воздух гелий |
|
Свойства веществ
Эти характеристики позволяют отличать одно вещество от другого, и их можно заметить без специальных приборов. Вы видите и ощущаете их в привычном состоянии: жидкую воду, твёрдый камень, газообразный воздух. Выделяют две основные группы свойств веществ: физические и химические.
Физические свойства
Их можно наблюдать и измерять без изменения химического состава вещества. Они описывают состояние и внешние характеристики и могут отвечать на вопрос «какое?»:
- Цвет. Например, медь имеет золотисто-розовый или красноватый оттенок, а золото — ярко-жёлтый.
- Запах. Уксусная кислота резкая, эфир чаще сладковатый, сера не имеет аромата.
- Агрегатное состояние. Твёрдое — олово, жидкое — йод, газообразное — углекислый газ.
- Плотность. Железо тонет в воде, потому что плотность у него выше, дерево плавает из-за более низкой плотности.
- Точка плавления и кипения. Вода замерзает при 0 °C и кипит при 100 °C, а ртуть замерзает при –38,83 °C.
- Электропроводность. Металлы, такие как медь и алюминий, хорошо проводят электричество, в то время как пластик — плохо.
- Растворимость. Сахар легко растворяется в воде, а песок нет.
Химические свойства
Эти характеристики проявляются только при химических реакциях, когда вещество вступает в контакт с другими веществами и изменяет свой состав:
- Реактивность с кислородом. Какие-то вещества не реагируют, например золото. Другие могут гореть, например дерево. Третьи — окисляться, как яблоко, которое темнеет, если его разрезать и оставить на столе.
- Реакция с кислотами. Металлы, такие как цинк, реагируют с кислотами, выделяют водород. А если смешать соду и уксус, то смесь будет шипеть и пузыриться. В результате образуется углекислый газ, вода и ацетат натрия.
- Горючесть. Бензин легко воспламеняется, а вода — нет.
- Коррозионная стойкость. Нержавеющая сталь устойчива к коррозии, в отличие от обычной стали.
Свойства вещества напрямую определяет его строение. Чтобы было проще понять, приведём пример. Графит в стержне для карандашей и алмаз состоят из одного и того же элемента — углерода (C). Однако их свойства кардинально различаются из‑за разного расположения атомов. В графите атомы образуют слои, которые легко скользят относительно друг друга, поэтому он мягкий и оставляет след на бумаге. В алмазе атомы соединены в жёсткую трёхмерную структуру, что делает его самым твёрдым известным в природе материалом.
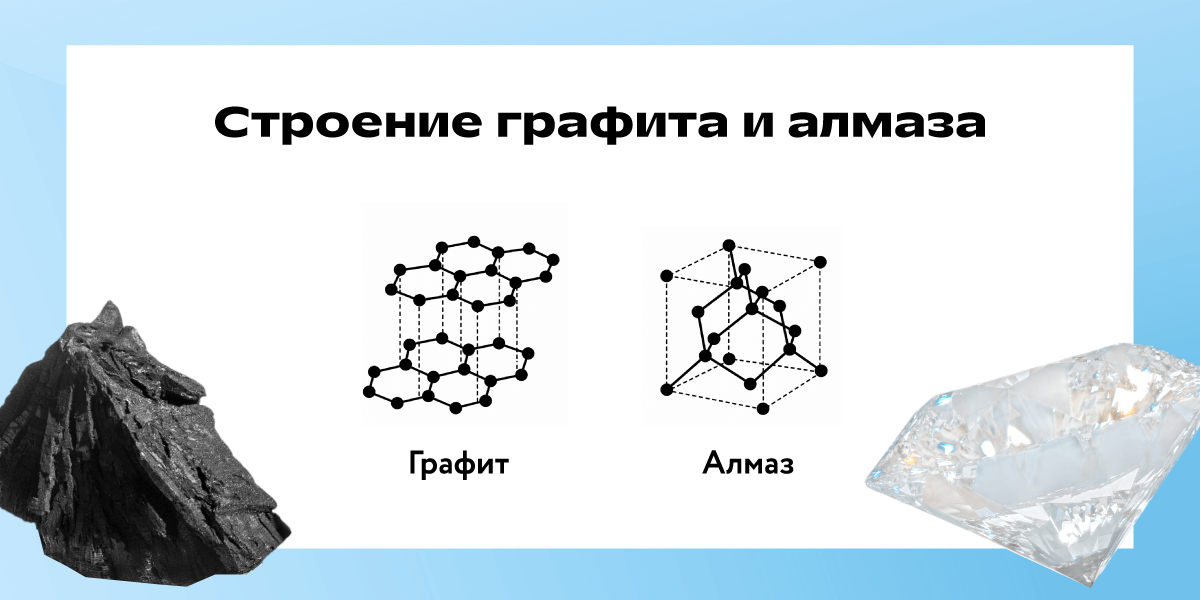
Цвет алмаза и графита зависит от их строения. Чистый алмаз прозрачен, так как его плотная решётка атомов углерода не поглощает свет. Графит чёрный или тёмно-серый — из-за слоистой структуры
Резюме
Эти знания полезны далеко за пределами урока в классе химии. Понимая, из чего состоят предметы вокруг и как они взаимодействуют друг с другом, человек начинает буквально «читать» окружающий мир. Повседневная жизнь наполняется причинно-следственными связями.
Становится понятно, что тесто поднимается, когда дрожжи или сода вступают в реакцию с другими компонентами, выделяя пузырьки углекислого газа. А сковороду лучше брать с пластиковой ручкой, потому что этот материал плохо проводит тепло. Такое базовое представление о веществах превращает всё вокруг из магии в осмысленный процесс.
Ответим на ваши вопросы
Свяжемся с вами в течение 5 минут и проведём бесплатную консультацию по вопросам перехода на домашнее обучение
Позвоним с 8 до 21 в рабочие дни









